全部で175問 挑戦中
【薬学理論】薬剤
-
溶解平衡
20%
※数字(%)は出題頻度
25℃において固相が十分に存在する条件下、pHと弱電解質Aの分子形とイオン形の溶解平衡時の濃度の関係を図に表した。以下の記述のうち、正しいのはどれか。2つ選べ。ただし、弱電解質Aの分子形とイオン形の溶解平衡時の濃度比はHenderson-Hasselbalchの式に従い、弱電解質Aの溶解やpH調整に伴う容積変化は無視できるものとする。必要ならば、log2=0.30、log3=0.48、101/2=3.2を用いて計算せよ。
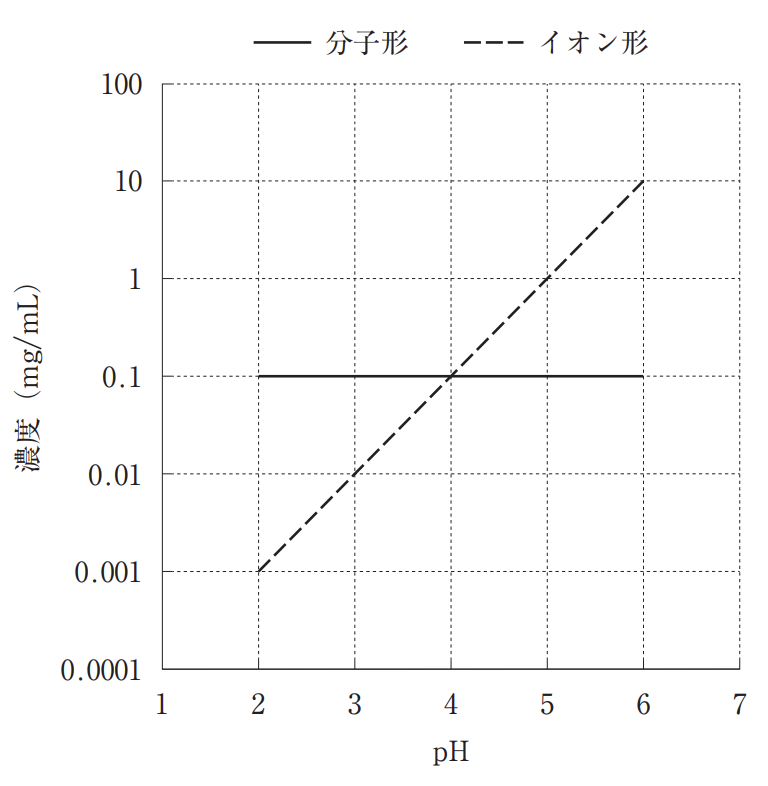
-
(1)
出題頻度について
- ・出題頻度は出題数÷公開中のテスト数となっています。
- ・出題頻度が50%なら、テストで2回に1回は出題されることになります。
- ・出題頻度が100を超える場合は、テストで1回以上必ず出題されることになります。
